Autor: Antonio Gutiérrez
-

Citomegalovirus
Hay un virus al que no le gusta la fama, no es como el SARSCov2, siempre en el candelero, siempre protagonista. Éste es más discreto, siempre en un segundo plano, nada de focos ni autógrafos. El citomegalovirus (CMV) es un género de herpesvirus que pertenece a la subfamilia Betaherpesvirinae, de la familia Herpesviridae ,concretamente herpesvirus…
-

Virus respiratorio sincitial
Esta entrada, algo más resumida, y con la colaboración de la Dra. Elena Salamanca, del Servicio de Enfermedades Infecciosas del Hospital Virgen Macarena de Sevilla, ha sido publicada en The Conversation El virus respiratorio sincitial (VRS) se descubrió en 1956 y sólo un año después ya se asoció como agente causal y principal responsable de…
-

Una pastillita para dormir
¿Conoces a alguien que NECESITE su ‘pastillita’ para dormir cada noche? Ésta es sólo la punta de un iceberg muy grande. Hoy tiramos del farmacéutico que hay por aquí Benzodiacepinas A toda esta familia de fármacos se les conoce por este nombre, pero en realidad el origen responde a la porción en la estructura química…
-
Automedicación e Interacciones medicamentosas
Qué son las interacciones medicamentosas y porqué no debemos automedicarnos.
-

Datos como protagonistas
Los datos se han hecho protagonistas. Asumámoslo. ¿Pero entendemos lo que cuentan? Les propongo un paseo por definiciones sencillas de medidas epidemiológicas básicas. En epidemiología usamos fundamentalmente 3 tipos de medidas: Frecuencia, asociación e impacto Para dar una breve clasificación: –Frecuencia: Prevalencia, Incidencia, Odds –Asociación: Riesgo relativo (RR) y Odds ratio (OR) –Impacto: Riesgo atribuible…
-
Evusheld: nuevo medicamento para profilaxis COVID19 en inmunodeprimidos
Leo que hay un poco de revuelo con el medicamento «Evusheld», la combinación de Acs monoclonales que previsiblemente esté disponible pronto (tixagevimab y cilgavimab). Me permito hacerles un breve repaso. De forma sencilla, los anticuerpos monoclonales son proteínas fabricadas en laboratorio que imitan la capacidad del sistema inmunitario para combatir patógenos nocivos como los virus.…
-

En el 200 º aniversario de su nacimiento, Louis Pasteur.
Hoy les hablaré de #epidemología. De pollos y cervezas. Y de un señor que quiso ser profesor de arte. Y que al final salvó millones de vidas En el 200 º aniversario de su nacimiento, Louis Pasteur. «Louis Pasteur no fue médico ni cirujano, pero nadie ha hecho tanto como él en favor de la…
-

Balmis y Zendal. La Real Expedición Filantrópica de la Vacuna
Como se acerca Navidad y la situación se torna delicada, os contaré la historia de cómo unos españoles llevaron el mejor regalo de Navidad posible, allende los mares. Una vacuna para ayudarlos a todos. Puede que no hayáis leído este hilo que enlazo abajo Habla de Edward Jenner, el descubridor de la vacuna para la…
-
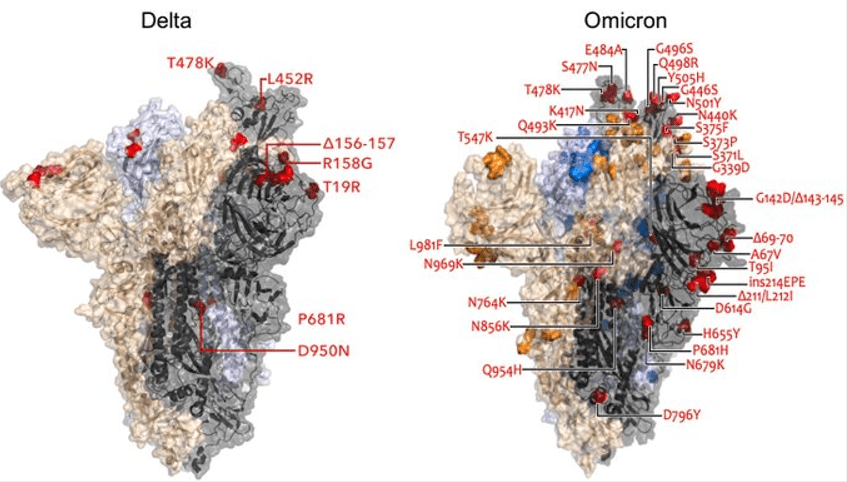
Omicron y la incertidumbre
RESUMEN de actualización a 10/12/2021 sobre #Omicron ¿Cómo se está dispersando? Aquí podemos ver porcentajes de identificación proporcionados por @GISAID and https://covariants.org Datos epidemiológicos preliminares procedentes de Gauteng indican que #omicron podría tener un Rt de entre ~ 0,8 a > 2. Esta cuestión descansa en buena medida en el % de susceptibles que tengamos.…
