Esta entrada, algo más resumida, y con la colaboración de la Dra. Elena Salamanca, del Servicio de Enfermedades Infecciosas del Hospital Virgen Macarena de Sevilla, ha sido publicada en The Conversation

El virus respiratorio sincitial (VRS) se descubrió en 1956 y sólo un año después ya se asoció como agente causal y principal responsable de la bronquiolitis.
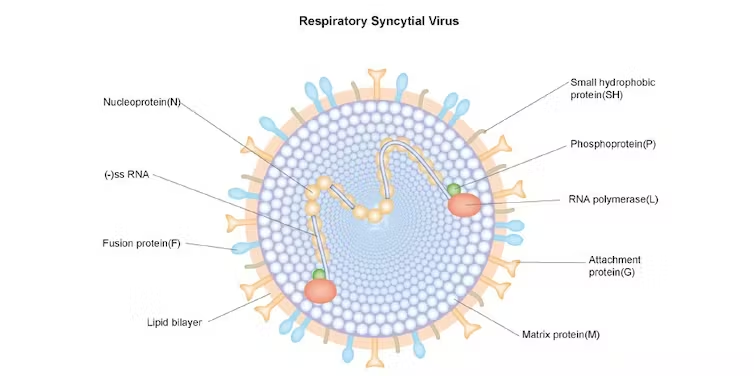
Estructuralmente, el VRS humano (nombre común), también conocido como orthopneumovirus humano, es un virus con envuelta lipídica y genoma constituido por una única molécula de ARN lineal, monocatenaria y de polaridad negativa.
Pertenece al género Orthopneumovirus, familia Pneumoviridae, orden Mononegavirales, de unas 15.000 bases de longitud, y que contiene 10 genes que codifican 11 proteínas estructurales y no estructurales.
Las más importantes son las glicoproteínas de fusión (F) y de adhesión (G) de la envuelta, cruciales para la infectividad y la patogenia del virus y que estimulan la producción de anticuerpos neutralizantes del huésped frente a la infección. La glicoproteína G es la responsable de la unión al receptor celular de la célula huésped.
Infección por el virus respiratorio sincitial y bronquiolitis ¿son lo mismo?
Este virus es la principal causa de infecciones en las vías respiratorias inferiores en la población infantil menor de un año, incluyendo bronquiolitis y neumonía, pero también en los adultos mayores de 65 años y en personas con condiciones de riesgo.
Se sabe que el 60-70% de los casos de bronquiolitis se deben a este virus, aunque existen otros que también pueden producir bronquiolitis (Rhinovirus, Metapneumovirus, Adenovirus, Bocavirus…).
La mayoría de los lactantes con infección por VRS solo tendrá síntomas leves y una enfermedad parecida al resfriado que se resuelve rápido. Pero algunas veces, después de 3-4 días con mocos y tos, puede ocasionar dificultad para respirar y “pitos” en el pecho, febrícula o fiebre, menos apetito, vómitos con mucosidad o dificultad para comer. El 50% de los recién nacidos que evolucionan a enfermedad grave son menores de 3 meses, y en su mayoría, son previamente sanos, siendo imprevisible conocer qué neonatos evolucionarán a casos graves.
Las personas mayores también se ven afectados por esta infección. Tienen mayor riesgo de gravedad debido a la inmunosenescencia (envenjecimiento del propio sistema inmune) y a otras enfermedades presentes. Además puede empeorar otras patologías, como la enfermedad pulmonar obstructiva crónica (EPOC), asma, o la insuficiencia cardíaca, y provocar complicaciones graves, como neumonía, hospitalización e incluso la muerte. A nivel mundial se estiman alrededor de 787,000 hospitalizaciones y 47.000 muertes anuales, relacionadas con el VRS, sólo en los países de altos ingresos.
Globalmente, es la segunda causa de muerte en el mundo en niños menores de un año, después de la malaria. En España, se hace vigilancia activa de las infecciones por este virus.
En esta temporada 2023-24, en la semana del 18 al 24 de diciembre a nivel de atención primaria, la tasa de infección por VRS se situaba en 129,5 casos por 100.000 habitantes (121,5/100.000 h en la semana previa); por grupos de edad, las mayores tasas se observaban en el grupo de 1 a 4 años (1637,5/100.000h), seguido de los menores de 1 año (888,4/100.000 h) y con una mediana de positividaden torno al 6%.
Además, hay que destacar que la infección por VRS se ha relacionado con sibilancias recurrentes, asma bronquial…y otras secuelas a largo plazo.

¿Qué hace a este año diferente de los anteriores?
Aquí vienen buenas noticias.
Como en muchas infecciones por virus, el tratamiento es únicamente sintomático, es decir, dirigido a disminuir los síntomas (manejo de secreciones, oxigenoterapia, hidratación y nutrición adecuadas, etc).
Por cierto, NO SIRVEN LOS ANTIBIÓTICOS, los jarabes para la tos, o los mucolíticos. En los casos graves, se recurre a terapia de soporte.
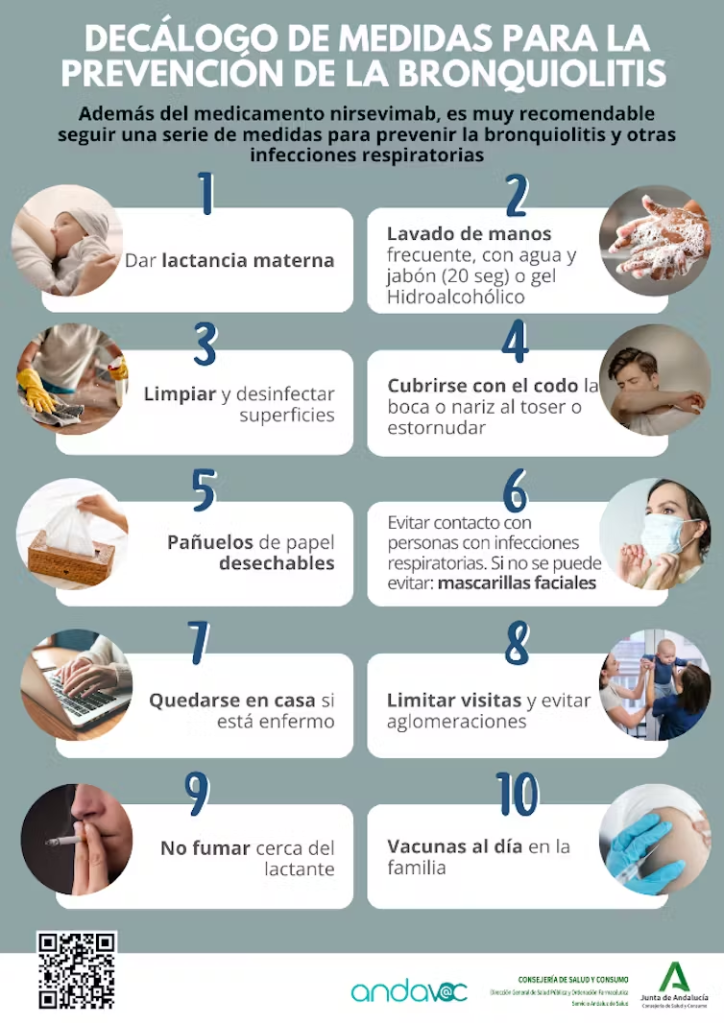
Hasta ahora, las medidas para prevenir esta infección se centraban en las disponibles para cualquier otro virus de similar mecanismo de transmisión, es decir, a través de aerosoles o gotitas que se producen al respirar, toser, estornudar, etc. También al tocar superficies u objetos en los que el VRS puede quedarse durante horas (chupetes, juguetes…) y tocar posteriormente la boca, la nariz o los ojos.
Medidas esenciales como el lavado de manos frecuente, uso de pañuelos de papel desechables (¡¡¡Y USARLOS SOLO UNA VEZ!!!), evitar que los adultos con infecciones respiratorias se acerquen al niño, o evitar el humo del tabaco y los ambientes muy concurridos.
Pero tras muchos años de investigación, contamos, por primera vez, con medidas con un impacto directo en la incidencia de esta enfermedad.
Mientras que durante la temporada 2022/2023 se popularizó el término “Tripledemia”, en esta temporada hemos conseguido una reducción del 83% de las hospitalizaciones en neonatología por VRS, y del 50% por otras infecciones respiratorias (infecciones neumocócicas, otitis media…).
Esto es debido a la popularmente llamada ‘vacuna del VRS’ para niños.
En realidad, no es una vacuna, sino un fármaco, de tipo ‘anticuerpo monoclonal’ que se llama Nirsevimab. (Beyfortus® (Sanofi). Estrictamente, este tipo de terapias se conocen como inmunización pasiva, que proporcionan protección más rápida puesto que se administra directamente el anticuperpo (Ac) al organismo, sin tener que esperar a que él mismo lo genere en respuesta a una vacuna.
Fue aprobado por el organismo europeo responsable de la regulación de este tipo de medicamentos, la agencia europea del medicamento (EMA) el 4 de noviembre de 2022.
Nirsevimab está diseñado para el epítopo θ de la configuración prefusión de la glicoproteína F o PreF (la forma en la que se encuentra antes de que el virus infecte la célula) y que con una sola inyección mantiene niveles protectores adecuados, reduciendo alrededor del 76 % la enfermedad de vías respiratorias bajas que precisa atención médica y de las hospitalizaciones, y del 78 % de las infecciones, en los 150 días siguientes a su administración.
Su aprobación se deriva de los resultados de eficacia y seguridad de dos ensayos clínicos multicéntricos aleatorizados, doble ciego, y comparados con placebo ([Fase IIb] y MELODY [Fase III]) para la prevención en lactantes a término y prematuros que se exponen a su primera temporada del VRS.
En nuestro país, está indicado para la prevención de la enfermedad de las vías respiratorias inferiores producida por el VRS en neonatos y lactantes durante su primera temporada del VRS. Hasta el momento, no está aprobado para adultos.

¿Qué resultados hemos visto tras su implantación?
Nirsevimab comenzó a administrarse a finales de septiembre de 2023 y la adherencia general ha sido muy favorable. En esas fechas, en la mayoría de Comunidades Autónomas de nuestro país (siguiendo las pautas del Ministerio) se llevaron a cabo campañas muy potentes y un calendario de inmunización muy ambicioso, que fue muy bien recibido por los padres de niños que cumplían criterios para recibir el fármaco. España es prácticamente pionera a nivel internacional, y, en vista de los resultados en vida real, debe ser motivo de orgullo.
La cobertura ‘vacunal’ (sabemos que no es ‘vacuna’ sino prevención mediante un medicamento) está siendo alta esta campaña 2023-24. En Andalucía se sitúa en torno al 94% en menores de 6 meses nacidos entre el 1 de abril de 2023 y 30 de septiembre de 2023, el 92,8% en lactantes nacidos desde el 1 de abril de 2023, en el 90,5% en lactantes prematuros de menos de 35 semanas, nacidos desde el 25 de septiembre de 2023 en adelante y del 91% en lactantes menores de 6 meses nacidos durante la temporada de VRS.
Otro ejemplo podría ser Galicia, con datos de cobertura del 85,7% en los nacidos entre el 1 de abril y el 24 de septiembre de 2023, y del 92.4% en los nacidos entre el 25 de septiembre y el 31 de diciembre de 2023.
Esta amplia cobertura ha redundado en una disminución clara de las tasas de hospitalización acumuladas en lactantes que recibieron nirsevimab comparado con estaciones anteriores y con los lactantes que no reciben el fármaco, suponiendo un descenso de hasta el 73% en la semana 48, la de mayor tasa de hospitalización, en comparación con la media de la misma semana de las 3 temporadas anteriores en época pre-covid, 2017-18, 2018-19 y 2019-20, en menores de 6 meses (96/100.000h vs. 339/100.000h), y del 80% (108/100.000h vs. 515/100.000h) en menores de 2 meses.
Además, una importantísima ventaja de esta molécula, es que tiene una vida media (duración de su efecto) mayor que otras anteriormente utilizadas, lo cual ha permitido que, con una única administración, dure su eficacia toda la temporada epidémica de VRS en los lactantes inmunizados.

Reflexión final
Los resultados observados este año con motivo de la introducción de un nuevo medicamento para la prevención de casos graves de infección por VRS han sido muy positivos. Han supuesto una caída brusca y significativa de la hospitalización y mortalidad, que este virus puede ocasionar en los niños más pequeños.
Es por ello necesario monitorizar los resultados que ofrece en siguientes ondas epidémicas, sin dejar de invertir en ciencia que ofrezca alternativas para éste y otros grupos de población vulnerables en caso de disminución de la efectividad, y sin dejar de lado estrategias de inmunización activa mediante vacunas, ya disponibles, como medida complementaria y necesaria para el control de esta infección y sus secuelas.
Deja un comentario