Etiqueta: epidemiologia
-

Citomegalovirus
Hay un virus al que no le gusta la fama, no es como el SARSCov2, siempre en el candelero, siempre protagonista. Éste es más discreto, siempre en un segundo plano, nada de focos ni autógrafos. El citomegalovirus (CMV) es un género de herpesvirus que pertenece a la subfamilia Betaherpesvirinae, de la familia Herpesviridae ,concretamente herpesvirus…
-

Virus respiratorio sincitial
Esta entrada, algo más resumida, y con la colaboración de la Dra. Elena Salamanca, del Servicio de Enfermedades Infecciosas del Hospital Virgen Macarena de Sevilla, ha sido publicada en The Conversation El virus respiratorio sincitial (VRS) se descubrió en 1956 y sólo un año después ya se asoció como agente causal y principal responsable de…
-

En el 200 º aniversario de su nacimiento, Louis Pasteur.
Hoy les hablaré de #epidemología. De pollos y cervezas. Y de un señor que quiso ser profesor de arte. Y que al final salvó millones de vidas En el 200 º aniversario de su nacimiento, Louis Pasteur. «Louis Pasteur no fue médico ni cirujano, pero nadie ha hecho tanto como él en favor de la…
-

Edward Jenner y la curiosidad
El 17 de mayo de 1749, nacía en la localidad inglesa de Berkeley Edward Jenner. con 21 años, Edward inició sus estudios en el Hospital de San Jorge de Londres, donde fue discípulo del famoso cirujano y anatomista John Hunter. Cuando Jenner regresó a Berkeley, la epidemia de viruela que afectaba a la población ya…
-

Medidas de mortalidad en epidemiología
Hoy les hablaré de #epidemiología. Y de mortalidad. Y de cómo medirla. «Si puede usted medir aquello de lo que habla y puede expresarlo con un número, sabe algo del tema, pero si no puede medirlo, su conocimiento es escaso» William Thomson Kelvin (1824-1907). La mortalidad, aunque la mayoría no quiera hablar sobre ella (salvo…
-
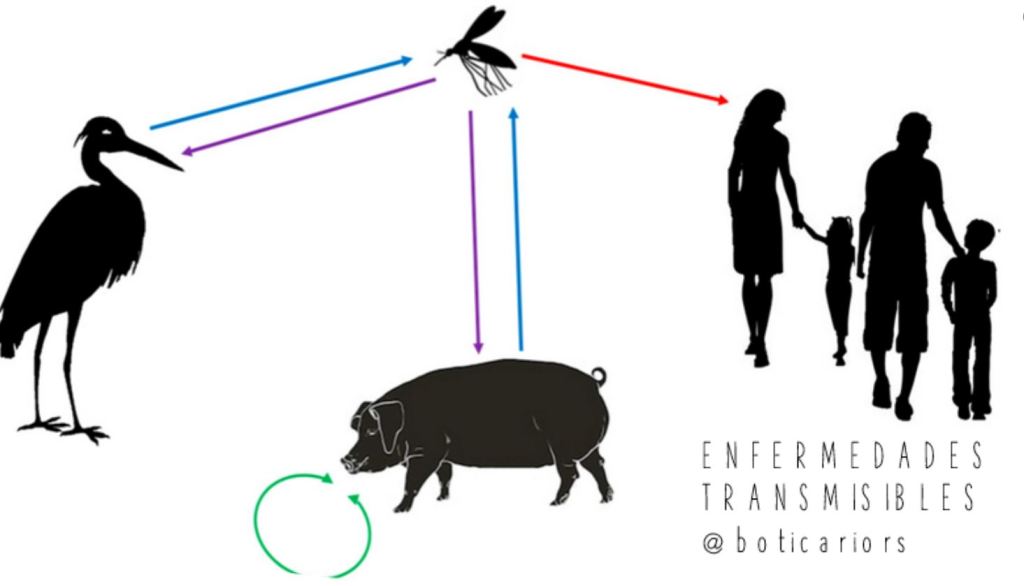
Las enfermedades transmisibles
Hoy les hablaré un poco sobre la epidemiología y control de las enfermedades trasmisibles, Si les apetece, están en su casa Primero, alguna definición claro (sé que es lo más rollo), pero breve. Enfermedad transmisible es la que precisa de un agente causal vivo, capaz de reproducirse y que provoca una respuesta en el organismo…
